Is – диаграмма водяного пара.
Is – диаграмма водяного пара.
Для практических расчетов процессов водяного пара широкое применение получила is-диаграмма, на которой теплота и энтальпия измеряются линейными отрезками.
В системе координат i—s (рис. 1) сначала строятся нижняя (а-К) и верхняя (К—с) пограничные кривые по табличным данным i и s. Нижняя пограничная кривая проходит через начало координат, так как при t=0 0 С энтропия и энтальпия приняты равными нулю.
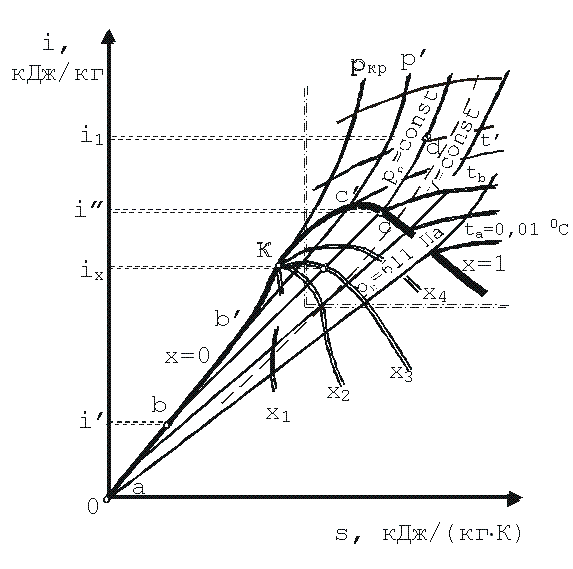 |
| Рис. 1. is-диаграмма водяного пара |
Затем наносят изобары, которые в области насыщенного пара, будучи одновременно и изотермами, являются прямыми линиями, так как при p=const, dq=di, а ds = dq/ T = di/ T.
Поэтому di=T·ds и при T=const, i=T·s+const. Следовательно, на is-диаграмме угловой коэффициент изобары равен T. Поэтому чем выше давление насыщения, тем выше температура T и тем больше тангенс угла наклона изобары. В области перегретого пара изобары и изотермы расходятся, причем изобары поднимаются кверху в виде логарифмических кривых, а изотермы стремятся к горизонтали. Это объясняется тем, что с понижением давления перегретый пар по свойствам приближается к идеальному газу, энтальпия которого зависит только то температуры, то есть линии t=const одновременно являются линиями i=const. Чем больше температура, тем выше расположена изотерма. В области влажного пара нанесены линии одинаковой степени сухости х=const. На эту же диаграмму часто наносят еще изохоры, которые проходят круче изобар. Is-диаграмма обладает рядом важных свойств: по ней можно быстро определить параметры пара и разность энтальпий в виде отрезков, наглядно изобразить адиабатный процесс, имеющий большое значение при изучении работы паровых двигателей, и решать другие задачи. Обычно для практического использования в большом масштабе строят так называемую рабочую часть диаграммы (на рис. 1. она ограничена штрих-пунктиром).
Процессы водяного пара на is-диаграмм: Как уже отмечалось, пар как реальный газ не подчиняется простым закономерностям идеальных газов, поэтому расчеты процессов с водяным паром проводятся с помощью таблиц или графически с помощью диаграмм.
Наиболее удобно оценивать характер изменения параметров разных процессов по is-диаграмме. Основные термодинамические процессы водяного пара (v=const, p=const, t=const) представлены на is-диаграмме соответствующими кривыми. Адиабатный процесс (s=const) изображается прямой, параллельной оси ординат. Следует обратить особое внимание на разные закономерности изменения параметров состояния пара в термодинамических процессах в зависимости от состояния пара (насыщенный или перегретый). Так, в изотермическом процессе в области насыщенного пара энтальпия изменяется значительно, а в области перегретого пара, особенно вдали от линии х=1, процесс t=const приближается к i=const. Это свидетельствует о том, что свойства перегретого пара в этих областях приближаются к свойствам идеального газа.
Температурное поле.
Температурное поле — совокупность значений температур во всех точках рассматриваемого пространства в данный момент времени. Для установившихся (стационарных) режимов Температурное поле от времени не зависит. Во многих случаях может рассматриваться зависимость Температурное поле от двух, а иногда от одной координаты. Графически Температурное поле изображают посредством изотермических поверхностей, соединяющих все точки поля с одинаковой температурой, а для двухмерного поля — посредством семейства изотерм. Расстояние между изотермами обратно пропорционально градиенту температуры; при этом скалярному Температурное поле соответствует векторное поле градиентов температуры После 2-го интегрирования: t = C1 x + C 2. Для определения констант интегрирования используем следующие формулы: при х =0, следует что t C 1 = C 2 ; при х = δ, получаем – t = tC 2 = C 1 * δ + C 2 = C 1 * δ + t C 1. Отсюда выразим С1: С1 = (t C 1 – tC 2 )/ δ .
Используя выражения определения С1 найдем t: t = tC1 – ((t C1 – tC2)/ δ)* x.
Изотермическая поверхность.
Изотермическая поверхность – это геометрическое место точек с одинаковой температурой. Изотермы не могут пересекаться, т.к. не может быть 2-х разных температур в точках в один и тот же момент времени. Они замыкаются сами на себя (t1 = const; t2 = const) и заканчиваются в окружающем пространстве (t3 = const). Если изотермические поверхности рассечь плоскостью, то в сечении получим изотермические линии, которые обладают теми же свойствами, что и изотермические поверхности.
Основные понятия о лучистом теплообмене. Лучистый поток. Плотность излучения, монохроматическое излучение, эффективное и результирующее излучение.
Тепловое излучение есть результат превращения внутренней энергии тел в энергию электромагнитных колебаний. При попадании тепловых лучей (волн) на другое тело их энергия частично поглощается им, снова превращаясь во внутреннюю. Так осуществляется лучистый теплообмен между телами. Тепловое излучение как процесс распространения электромагнитных волн характеризуется длиной волны λ и частотой колебаний ν = c /λ , где с — скорость света.
Все виды электромагнитного излучения имеют одинаковую природу, поэтому классификация излучения по длинам волн в зависимости от производимого ими эффекта носит лишь условный характер. При температурах, с какими обычно имеют дело в технике, основное количество энергии излучается при длине волны 0,8-80 мкм. Эти лучи принято называть тепловыми (инфракрасными). Тепловой поток, излучаемый на всех длинах волн с единицы поверхности
тела по всем направлениям, называется поверхностнойплотностью потокаинтегрального излучения Е, Вт/м2. Она определяется природой данного тела и его температурой. Это собственное излучение тела. Часть энергии излучения Е пад, падающей на тело, поглощается (ЕА), часть отражается (ER) и часть проникает сквозь него (ED). Таким образом, ЕА + ER + ED
Это уравнение теплового баланса можно записать в безразмерной форме: A+R+D=1 .
А = ЕА/ Е пад — коэффициент поглощения, E=ER/ Е пад — коэффициентом отражения, D = ED/ Е пад – коэффициентом пропускания.
Тело, поглощающее все падающее на него излучение, называется абсолютночерным. Для этого тела А = 1. Тела, для которых коэффициент А 0 С энтропия и энтальпия приняты равными нулю.
 |
| Рис. 1. is-диаграмма водяного пара |
Затем наносят изобары, которые в области насыщенного пара, будучи одновременно и изотермами, являются прямыми линиями, так как при p=const, dq=di, а ds = dq/ T = di/ T.
Поэтому di=T·ds и при T=const, i=T·s+const. Следовательно, на is-диаграмме угловой коэффициент изобары равен T. Поэтому чем выше давление насыщения, тем выше температура T и тем больше тангенс угла наклона изобары. В области перегретого пара изобары и изотермы расходятся, причем изобары поднимаются кверху в виде логарифмических кривых, а изотермы стремятся к горизонтали. Это объясняется тем, что с понижением давления перегретый пар по свойствам приближается к идеальному газу, энтальпия которого зависит только то температуры, то есть линии t=const одновременно являются линиями i=const. Чем больше температура, тем выше расположена изотерма. В области влажного пара нанесены линии одинаковой степени сухости х=const. На эту же диаграмму часто наносят еще изохоры, которые проходят круче изобар. Is-диаграмма обладает рядом важных свойств: по ней можно быстро определить параметры пара и разность энтальпий в виде отрезков, наглядно изобразить адиабатный процесс, имеющий большое значение при изучении работы паровых двигателей, и решать другие задачи. Обычно для практического использования в большом масштабе строят так называемую рабочую часть диаграммы (на рис. 1. она ограничена штрих-пунктиром).
Процессы водяного пара на is-диаграмм: Как уже отмечалось, пар как реальный газ не подчиняется простым закономерностям идеальных газов, поэтому расчеты процессов с водяным паром проводятся с помощью таблиц или графически с помощью диаграмм.
Наиболее удобно оценивать характер изменения параметров разных процессов по is-диаграмме. Основные термодинамические процессы водяного пара (v=const, p=const, t=const) представлены на is-диаграмме соответствующими кривыми. Адиабатный процесс (s=const) изображается прямой, параллельной оси ординат. Следует обратить особое внимание на разные закономерности изменения параметров состояния пара в термодинамических процессах в зависимости от состояния пара (насыщенный или перегретый). Так, в изотермическом процессе в области насыщенного пара энтальпия изменяется значительно, а в области перегретого пара, особенно вдали от линии х=1, процесс t=const приближается к i=const. Это свидетельствует о том, что свойства перегретого пара в этих областях приближаются к свойствам идеального газа.
Источник статьи: http://infopedia.su/22xba5a.html
Диаграммы водяного пара
Здравствуйте! Определять параметры и функции состояния по формулам зачастую бывает затруднительно вследствие сложной зависимости теплоемкости водяного пара и теплоты парообразования от температуры и давления. Поэтому для водяного пара, на основании экспериментальных исследований составлены таблицы, отражающие зависимости важнейших параметров водяного пара. Пользуясь ими, к примеру, по известному давлению сухого насыщенного пара можно определить все остальные параметры.
Так как состояние сухого насыщенного пара однозначно определяется его давлением р или температурой насыщения Тн, то таблицы составляются по давлению или температуре. По одному из этих параметров из таблиц можно определить другие величины, характеризующие состояние сухого насыщенного пара. В таблицах перегретого пара приводятся его параметры и функции состояния в зависимости от температуры и давления пара.
Расчет процессов изменения состояния пара упрощается при переходе к графическому методу, основанному на использовании диаграмм состояния. В этом случае не требуется проводить большой объем вычислений и расчет сводится к определению параметров с помощью диаграмм. Графическим методом легко определить не только начальные и конечные параметры пара в процессе, но и все промежуточные параметры состояния, что существенно упрощает инженерные расчеты.
Преимуществом графического метода является возможность сравнительно просто проследить связь между различными величинами, это делает его незаменимым при теоретическом анализе различных процессов в тепловых двигателях. С помощью диаграммы, как и по таблицам, можно определить параметры и функции состояния водяного пара, в том числе и влажного насыщенного пара.
Наибольшее распространение получили Ts- и is-диаграммы состояния водяного пара. Так как с помощью Ts-диаграммы легко определить количество теплоты в процессе, то она и применяется в основном для теоретического анализа экономичности тепловых двигателей. При расчетах различных процессов изменения состояния используется главным образом is- диаграмма водяного пара.
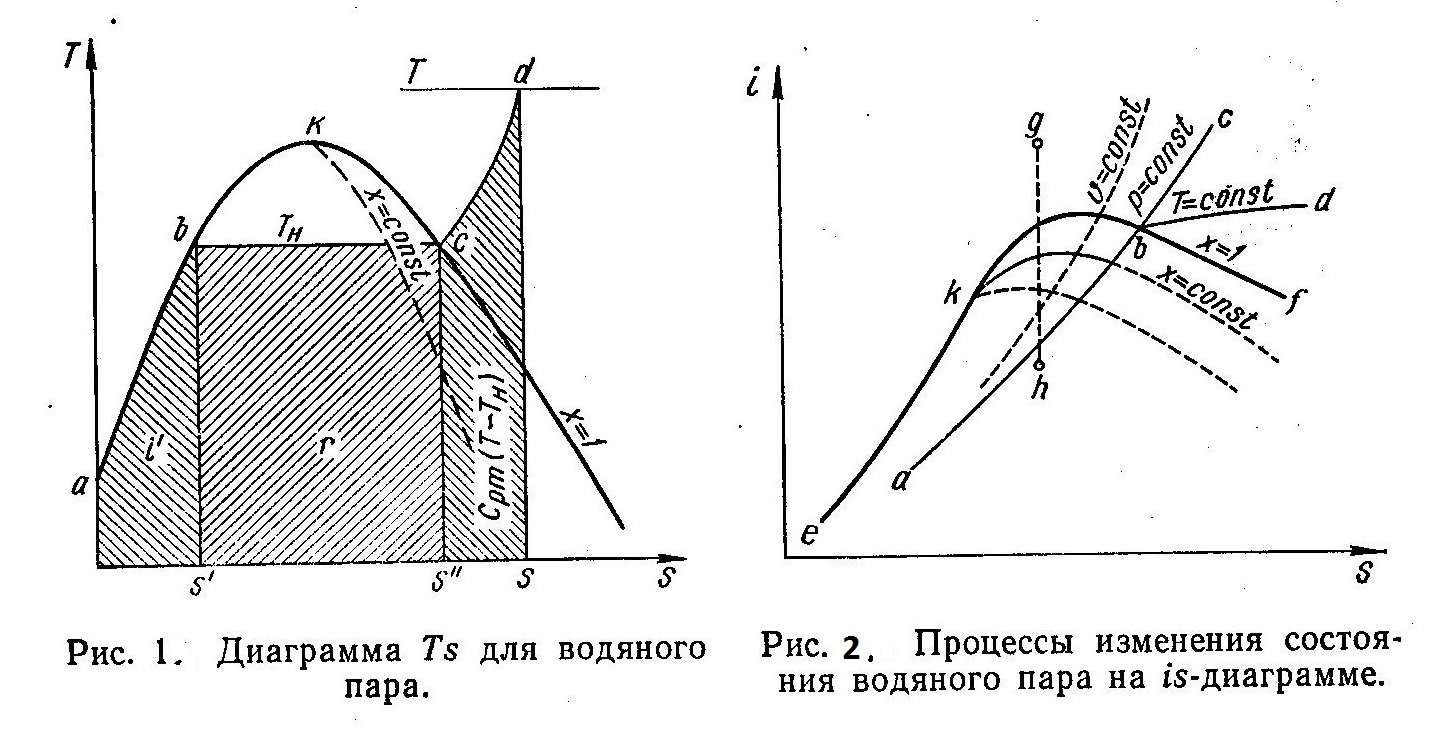
На рис. 1 в координатах Ts изображен процесс парообразования при р = const (процесс abcd). Кривая аКс является пограничной кривой, а точка К — критической точкой. Начало отсчета энтропии соответствует ее значению при 273 К. Площадь под кривой процесса на is-диаграмме соответствует количеству теплоты.
Следовательно, площадь под изобарой ab эквивалентна энтальпии воды i’ при температуре парообразования Tн. На изобарном участке bс, совпадающем с изотермой, происходит процесс парообразования, и площадь под прямой bс соответствует теплоте парообразования г. В изобарном процессе перегрева cd температура пара повышается до значения Т, и к пару подводится количество теплоты срm (Т—Тн). Линии постоянной степени сухости х=const, как и на всех диаграммах, сходятся в критической точке К.
На рис. 2 показаны различные процессы изменения состояния водяного пара на is-диаграмме. Область диаграммы, расположенная левее пограничной кривой еК, соответствует состоя-нию жидкости. Пограничная кривая пара Kf делит диаграмму на две области. Выше этой кривой расположена область перегретого пара, а ниже — область влажного пара. На пограничной кривой Kf пар является сухим насыщенным (х=1). Изобарный процесс изображен линией abc, изотермический — abd (в области влажного пара изотерма и изобара совпадают), изохорный — υ=const и адиабатный — gh. Кроме того, на этом рисунке показаны линии постоянной степени сухости х = const. В таблицах и на диаграммах не приводятся значения внутренней энергии газа, которую можно определить из соотношения u = i—pυ.
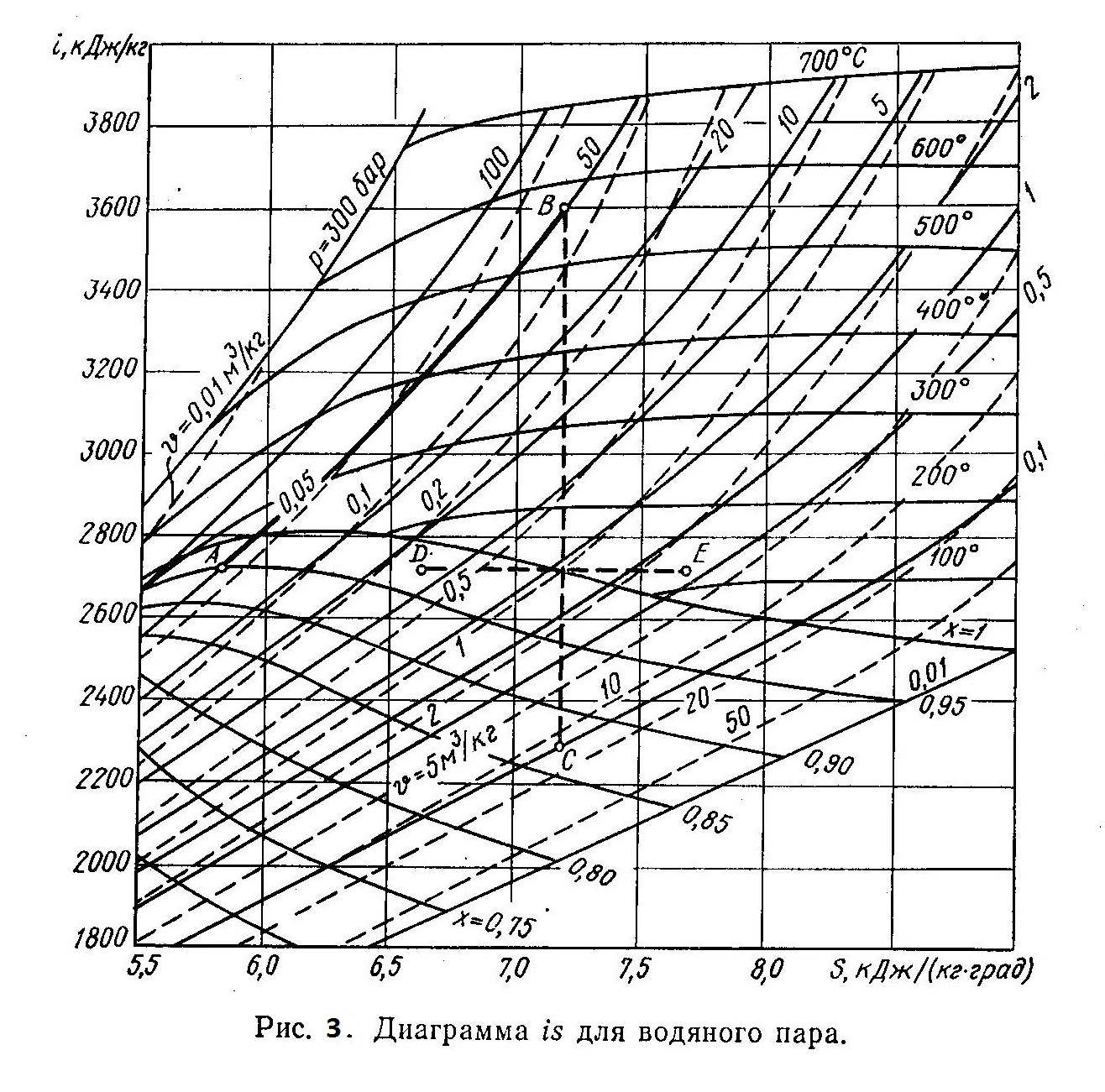
На рис. 3 приведена is-диаграмма водяного пара. При графическом расчете процессов по любым двум известным величинам (р, υ, Т; х, i, s) находят на диаграмме точку, соответствующую начальному состоянию пара, и все неизвестные параметры. Конечное состояние пара можно определить также по двум известным параметрам состояния. Если задан только один конечный параметр состояния, то необходимо знать еще характер процесса. В этом случае точку, характеризующую конечное состояние, находят на пересечении заданной кривой процесса и соответствующей изопараметрической кривой, например изобары.
Пример. Определить количество теплоты, сообщаемой 1 кг пара в пароперегревателе котельного агрегата. Начальные параметры пара p1 = 5 МПа и x1=0,95. Известно также, что после адиабатного расширения пара в турбине х2 = 0,87, а конечное давление пара р2=0,01 МПа.
Решение. Так как в пароперегревателе к пару подводится теплота при постоянном давлении, то количество ее равно разности начальной энтальпии i1 и энтальпии i2 пара после пароперегревателя: q=i2—i1. По начальным параметрам пара p1 и x1 на is-диаграмме находим точку А (рис. 3), которой соответствует значение энтальпии i1=2720 кДж/кг. Точку В, соответствующую состоянию пара на выходе из пароперегревателя, находим на пересечении изобары p1=5 МПа и адиабаты ВС, которая проходит через точку С. Положение точки С определяется параметрами пара р2 и x2. Энтальпия пара в точке В i2 = 3600 кДж/кг.
Количество подведенной к 1 кг пара теплоты равно q = 3600—2720=880 кДж/кг. Рассмотренный пример показывает, что is-диаграмма значительно упрощает расчеты процессов для водяного пара. Исп.литература: 1) Теплотехника и теплотехническое оборудование предприятий промышленности строительных материалов и изделий, Н.М. Никифорова, Москва, «Высшая школа», 1981. 2) Теплотехника, Бондарев В.А., Процкий А.Е., Гринкевич Р.Н. Минск, изд. 2-е,»Вышейшая школа», 1976.
Источник статьи: http://teplosniks.ru/texnicheskaya-termodinamika/diagrammy-vodyanogo-para.html